Diagnostische Marker im Stuhl und was sie bedeuten
Im Stuhl gibt es eine Vielzahl von biochemischen Markern, die Aufschluss über Entzündungen, den Zustand der Darmschleimhaut, die Verdauungsleistung und die Immunabwehr des Darms geben können.
Entzündungsmarker
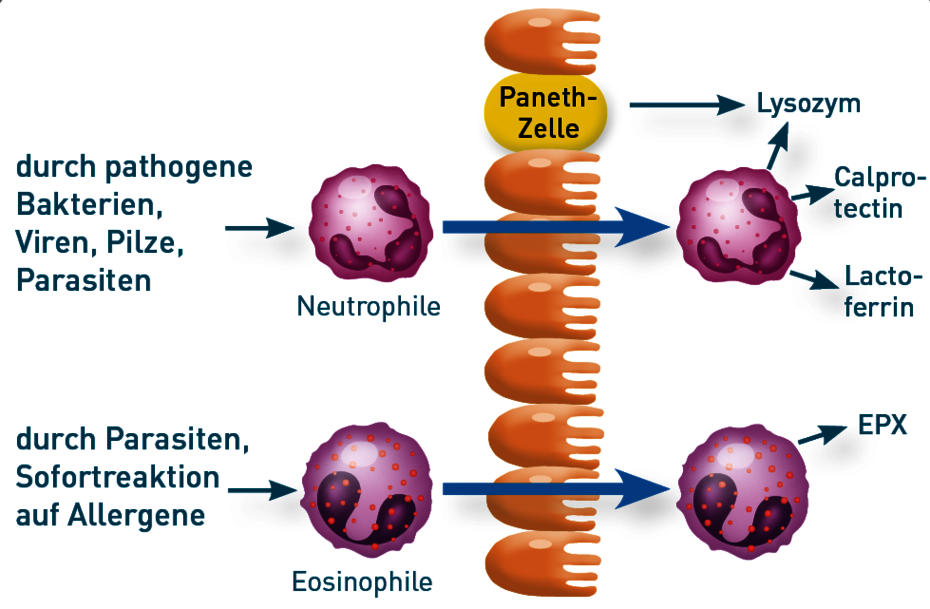
Das Vorliegen einer akuten Entzündung im Darm lässt sich über die Diagnostik von Calprotectin nachweisen. Calprotectin ist ein Calcium- und Zink-bindendes Protein mit antimikrobiellen Eigenschaften. Es ist ein Bestandteil von neutrophilen Granulozyten. Erhöhte Werte im Stuhl sind daher ein Zeichen einer vermehrten Einwanderung von Granulozyten in das Darmlumen. Das geschieht als Reaktion auf Entzündungsreize, z.B. bei Infektionen, einer Dysbiose mit vielen proinflammatorischen Bakterien, Divertikulitis oder Neoplasien. Der Marker ist zur Erkennung von entzündlichen Darmerkrankungen und zu ihrer Verlaufskontrolle geeignet. Erhöhte Calprotectin-Werte im Stuhl (> 50 µg/g) sind bei Morbus Chron und Colitis Ulcerosa, nicht aber bei Reizdarm beschrieben worden.
Lactoferrin ist ein eisenbindendes Protein, das, wie Calprotectin, von neutrophilen Granulozyten gebildet wird. Lactoferrin hat antimikrobielle, antivirale und antioxidative Eigenschaften. Da es Bestandteil der Muttermilch ist, ist Lactoferrin bei Säuglingen allerdings kein geeigneter Entzündungsmarker.
Die Ausschüttung von Lysozym in den Darm wird durch Bakterien induziert. Das Enzym schädigt bakterielle Zellwände und Membranen. Lysozym wird bei Pathogenkontakt von Paneth-Zellen im Dünndarm ausgeschüttet sowie von Neutrophilen und Makrophagen produziert.
Eosinophiles Protein X (EPX oder EDN für Eosinophil Derived Neurotoxin) wird von eosinophilen Granulozyten gebildet, die unter anderem an der Abwehr von Parasiten (v.a. Wurmparasiten) und an allergischen Reaktionen beteiligt sind. Bei Nahrungsmittelallergien vom Soforttyp, aber auch bei Parasitenbefall und Darmentzündungen werden erhöhte Werte für EPX im Stuhl gemessen.
Marker der Immunabwehr
Der gesunde Darm beherbergt Hunderte von nicht-pathogenen (kommensalen) Bakterienarten, ist gleichzeitig aber eine wichtige Eintrittspforte für Pathogene. Die wichtigste Aufgabe des intestinalen Immunsystems ist es daher, Pathogene von Kommensalen zu unterscheiden, erstere abzuwehren und letztere zu tolerieren. Diese adaptive Immunität spielt eine entscheidende Rolle bei der Aufrechterhaltung der Wirts-Mikrobiota-Homöostase. Ein Hauptmerkmal der adaptiven Immunantwort an Schleimhäuten ist die Sekretion von Immunglobulin A. Das sekretorische IgA (sIgA) bietet entscheidenden Schutz gegen Krankheitserreger und Toxine und kann Bakterien direkt binden und damit ihre Ausscheidung fördern.
Eine wichtige Komponente der angeborenen Immunantwort sind antimikrobielle Peptide, die gegen verschiedene Infektionserreger wirksam sind. Zu diesen Molekülen gehört ß-Defensin 2, das in verschiedenen Epithelien, so auch im Darmepithel, gebildet wird. Die Expression von ß-Defensin 2 wird durch Bakterien, Parasiten und Enterotoxine, sowie durch einige proentzündliche Zytokine induziert. Es gibt Hinweise darauf, dass die Kombination der Marker Calprotectin und ß-Defensin 2 die Diagnostik chronisch-entzündlicher Darmerkrankungen in Abgrenzung zum Reizdarm-Syndrom verbessern kann.
Marker für die Integrität der Darmschleimhaut
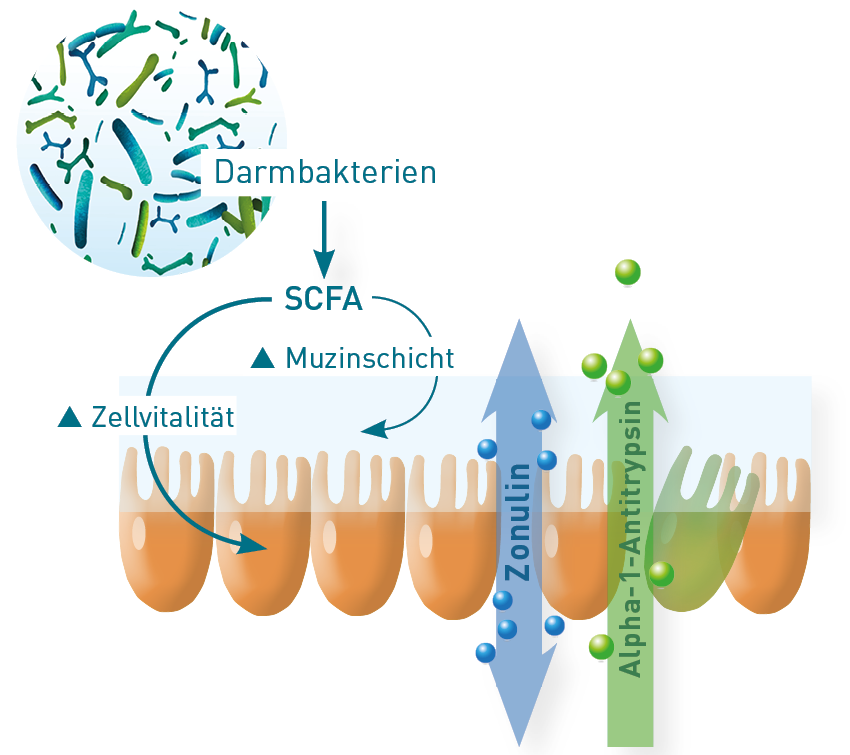
Die Festigkeit der Zell-Zell-Verbindungen der Darmschleimhaut (tight junctions) wird, soweit bekannt, über proinflammatorische Zytokine und über Zonulin-Peptide reguliert. Zonulin ist ein humanes Homolog zum Zonula-OccludensToxin, ein in Vibrio cholera entdecktes Enterotoxin, das in der Lage ist, intrazelluläre tight junctions reversibel zu öffnen. Die Ausschüttung von Zonulin kann durch pathogene Bakterien, einige Nahrungsmittelantigene, insbesondere Weizenbestandteile sowie durch proentzündliche Zytokine (TNF-alpha) induziert werden. Eine unkontrollierte Mehrausschüttung von Zonulin schafft dauerhafte Lücken im Darmepithel (leaky gut) und ermöglicht es größeren Molekülen, wie bakteriellen Metaboliten und Nahrungsmittelantigenen, das Darmlumen zu verlassen. Erhöhte ZonulinWerte wurden unter anderem bei Patienten mit Morbus Chron, Morbus Parkinson, Reizdarmsyndrom und Zöliakie gefunden.
Eine erhöhte intestinale Permeabilität (leaky gut) kann im Stuhl auch durch Messung von Alpha-1-Antitrypsin nachgewiesen werden. Alpha-1-Antitrypsin ist ein Plasmaprotein mit hohem Molekulargewicht. Es geht nur bei erhöhter Schleimhautpermeabilität passiv in den Stuhl über. Erhöhte Werte sind leaky-gut-, aber nicht entzündungsspezifisch.
Kurzkettige Fettsäuren (SCFA) wie Acetat, Butyrat und Propionat werden von bestimmten Darmbakterien gebildet und spielen eine entscheidende Rolle bei der Aufrechterhaltung der Barrierefunktion des Darms und der Abwehr von Krankheitserregern. Butyrat ist für die Energiebildung in Kolonozyten essenziell und beeinflusst damit maßgeblich die Zellvitalität im Darmepithel. Sie induzieren außerdem die Schleimbildung zum Erhalt der Muzinschicht, die als mechanische Abwehrzone die Epithelzellen vor dem Kontakt mit proentzündlichen Molekülen schützt. SCFA sind deshalb ebenfalls ein wichtiger Stuhlmarker bei der Beurteilung der Integrität der Darmbarriere.
Marker für die Verdauungsleistung
Die Messung von Verdauungsrückständen, also unverdauter Fette, Eiweiße und Zucker kann einen Hinweis auf das Vorliegen von Fehlfunktionen der Fett-, Protein- und Kohlehydratverdauung geben.
Grund dafür kann z.B. eine exokrine Pankreasinsuffizienz sein. Um diese festzustellen, kann im Stuhl die Pankreaselastase (auch Elastase-1) gemessen werden. Es handelt sich um ein proteolytisches Enzym, das im Gegensatz zu anderen Pankreasenzymen während seiner Passage durch den Darm nicht abgebaut wird. Studien haben gezeigt, dass die Messung dieses Enzyms gut mit der Produktion anderer Pankreasenzyme wie Amylase, Lipase und Trypsin korreliert.
Gallensäuren sind für die Fettverdauung im Dünndarm essenziell. Sie emulgieren Nahrungsfette und machen sie so für Lipasen zugänglich. Sie werden im enterohepatischen Kreislauf zu ca. 95 % im terminalen Ileum resorbiert und zurück zur Leber transportiert. Erhöhte Werte im Stuhl zeigen an, dass diese Rückresorption gestört ist oder zu viele Gallensäuren von der Leber produziert werden. Das kann Diarrhoe und Schleimhautreizungen zur Folge haben. Eine Malabsorption von Gallensäuren wurde bei 30 % der Patienten mit Reizdarmsyndrom-Diarrhoe diagnostiziert.
Bei einem Mangel an Gallensäuren im Dünndarm, sei es durch eine Gallensäuremalabsorption oder eine zu geringe Bildung bzw. Ausschüttung in den Darm, kann es zu einer Beeinträchtigung der Fettverdauung kommen. Dabei werden auch fettlösliche Vitamine weniger gut resorbiert.
Material
Wir benötigen zwei zu je 2/3 befüllte Stuhlröhrchen.
Um lagerungsbedingte Veränderungen zu vermeiden, sollte der Transport der Stuhlröhrchen ins Labor zeitnah und per Kurier erfolgen. Bitte ordern Sie unseren kostenfreien Kurier unter Tel. +49 30 77001-450.
Abrechnung
Eine Abrechnung ist bei gegebener Indikation für die Marker Alpha-1-Antitrypsin, Calprotectin, Lactoferrin, Lysozym, Gallensäuren und Pankreaselastase im kassen- und privatärztlichen Bereich gegeben. Die Abrechnung von ß-Defensin, EPX, kurzkettigen Fettsäuren, sIgA, Verdauungsrückständen, und Zonulin ist nur im privatärztlichen Bereich (GOÄ) gegeben. Selbstzahler entnehmen die Kosten für die einzelnen Analysen bitte dem Anforderungsschein Mikrobiom Selbstzahler.
Literatur
- Farrugia, Alexia, and Ramesh Arasaradnam. „Bile acid diarrhoea: pathophysiology, diagnosis and management.“ Frontline Gastroenterology 12.6 (2021): 500-507.
- Fasano, Alessio. „Intestinal permeability and its regulation by zonulin: diagnostic and therapeutic implications.“ Clinical Gastroenterology and Hepatology 10.10 (2012).
- Gacesa, R., et al. „A combination of fecal calprotectin and human betadefensin 2 facilitates diagnosis and monitoring of inflammatory bowel disease.“ Gut Microbes 13.1 (2021): 1943288.
- Ganz, T. „Lysozyme.“ (2006): 649-653. • Kovalszki, Anna, and Peter F. Weller. „Eosinophils and eosinophilia.“ Clinical immunology. Elsevier, 2019. 349-361.
- Rogier, Eric W., et al. „Secretory IgA is concentrated in the outer layer of colonic mucus along with gut bacteria.“ Pathogens 3.2 (2014).
- Siddiqui, Imran, Hafsa Majid, and Shahab Abid. „Update on clinical and research applica-tion of fecal biomarkers for gastrointestinal diseases.“ World journal of gastrointestinal pharmacology and therapeutics 8.1 (2017): 39.
- Vernia, Filippo, et al. „Is fecal calprotectin an accurate marker in the management of Crohn‘s disease?.“ Journal of gastroenterology and hepatology 35.3 (2020).