Nachweis neutralisierender Antikörper auf SARS-CoV-2 mit dem Surrogat-Virus-Neutralisationstest
Infolge einer Infektion mit dem SARS-CoV-2 Virus oder nach einer Impfung gegen selbiges Virus bildet das Immunsystem für gewöhnlich verschiedene Antikörper. Diese SARS-CoV-2-spezifischen Antikörper (-IgM, -IgA und/oder –IgG) können in medizinischen Laboren routinemäßig bestimmt werden. Für die Frage der durchgemachten Infektion sowie der Frage nach erwünschter Antikörperbildung nach Impfung ist das ausreichend. Eine Einschätzung der tatsächlichen Schutzwirkung (nach Infektion oder Impfung) ist durch die Antikörperbestimmung allein aber nur eingeschränkt möglich. Denn nur ein Teil der Antikörper ist in der Lage, hemmend auf die biologische Aktivität des Virus zu wirken. Diese Antikörper werden neutralisierende Antikörper genannt. Sie binden an zentrale Oberflächenstrukturen des Virus und blockieren so die Bindung der Viren an die menschliche Wirtszelle. So wird die zelluläre Infiltration und die Virus-Replikation vermieden.
Wie teste ich die Neutralisationskapazität von Antikörpern
Der Goldstandard für die Überprüfung dieser neutralisierenden Eigenschaften von Antikörpern ist der Plaque-Reduktions-Neutralisationstest (PRNT), welcher bisher im niedergelassenen Bereich allerdings nicht möglich war. Dieser Test erfordert einen S3-Sicherheitsstandard (Umgang mit vermehrungsfähigen Viren), den lediglich virologische Speziallabors an Universitätskliniken gewährleisten können.
Jetzt gibt es eine Alternative.
Mit dem Surrogat-Virus-Neutralisationstest (sVNT) ist es möglich, in einem ELISA-Testformat die inhibitorische Wirkung neutralisierender Antikörper innerhalb kürzester Zeit nachzuweisen (Tan et al., 2020). Dieser Test steht im IMD zur Verfügung.
Das Testprinzip des Surrogat-Virus-Neutralisationstests
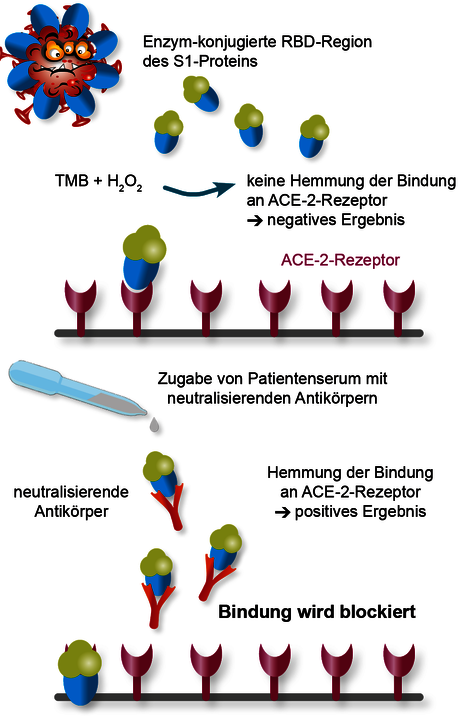
Beim SARS-CoV-2-Neutralisationstest ist die ELISA-Platte mit dem humanen ACE2-Rezeptor beschichtet. Das Serum des Patienten wird mit einem RBD-Fragment des viralen S1-Proteins inkubiert. Sofern im Serum Antikörper vorhanden sind, welche das S1-Protein binden („neutralisieren“) können, wird im 2. Schritt die Bindung an die ACE2-Rezeptoren verhindert. Nach mehreren Waschschritten, der Färbereaktion (mit TMB) und der photometrischen Messung wird die Hemmung der RBD-Fragment-Bindung in Prozent berechnet.
Studien zeigen hervorragende Korrelation zum PlaqueReduktions-Neutralisationstest (PRNT).
Verschiedenste Publikationen zeigen, dass die Ergebnisse des Surrogat-Virus-Neutralisationstests sehr gut mit dem Plaque-Reduktions-Neutralisationstests (PRNT) korrelieren (Chee Wah Tan et). Dabei kann ein cut off von 30% Neutralisationsfähigkeit eine hervorragende Differenzierung zwischen positiven und negativen Serumproben ermöglichen (Sean C. Taylor et. al.).
Es stehen zwei Testvarianten für verschiedene Indikationen zur Verfügung
Indikation 1: Kontrolle der Immunität durch die Impfung
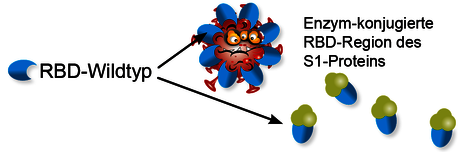
Alle bisher in Europa zugelassenen Impfstoffe basieren ausschließlich auf dem Spikeprotein der Wildtyp-SARS-CoV2-Viren (ursprüngliche Variante). Durch Verwendung des RBD-Fragments des S1-Proteins der Wildtypvariante kann somit effizient getestet werden, ob eine erwünschte und deutliche humorale Immunität entstanden ist.
Vom Wildtyp des Virus bis hin zur Delta-Variante korrelierte dabei die Höhe der IgG (S1)-Ak-Titer sehr gut mit der Neutralisationskapazität. Allerdings kann es bei niedrigen und mittleren Antikörpertitern durchaus zu erheblichen Unterschieden kommen.
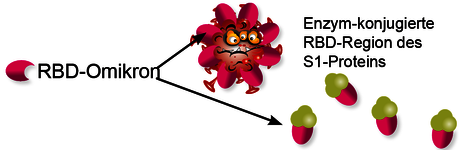
Indikation 2: Antikörper-Schutz gegenüber der OmikronVariante
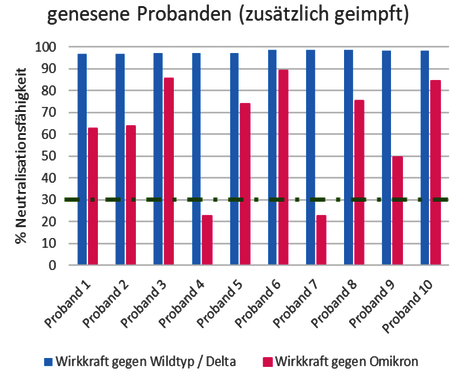
Die Omikron-Variante ist die aktuell vorherrschende Variante des SARS-CoV-2-Virus und ist weitaus ansteckender und weist impfstoffresistente Mutationen auf (Jiahui Chen et al. 2022; Hoffmann et al. 2022). Die starke Infektiosität und die teilweise Antikörperresistenz der Variante wird durch zahlreiche Mutationen in der rezeptorbindenden Domäne (RBD) des Spike-Proteins hervorgerufen. Somit passen die zuvor durch die Impfung oder Infektion (nicht Omikron-Variante) generierten IgG (S1)-Ak nicht mehr exakt und verlieren dadurch ihre Bindungs- und somit auch ihre Neutralisationsfähigkeit. Eine hohe Neutralisationskapazität gegen den Wildtyp bedeutet also nicht zwangsweise auch eine hohe Schutzwirkung gegenüber der aktuell vorherrschenden Omikron-Variante (Abb 3). Durch eine Modifikation des Surrogat-Neutralisationstests mit Verwendung des RBD-Fragments der Omikron-Variante können nun aber gezielt Rückschlüsse gezogen werden auf die tatsächliche Schutzwirkung der Ak gegenüber Omikron
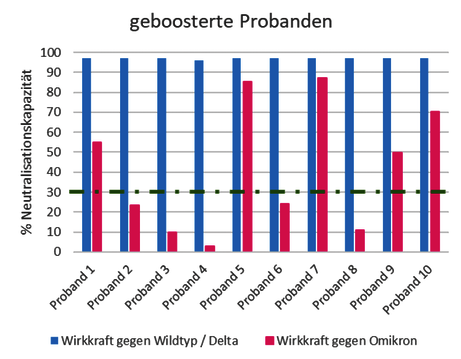
Referenzbereich Surrogat-Neutralisationstest (< 30% keine signifikante Neutralisationskapazität)
Abb. 3 Varianz in der Neutralisationsfähigkeit SARS-CoV-2-spezifischer AK gegenüber Wildtyp- und Delta-Variante im Vergleich zur Omikron-Variante bei geboosterten und genesenen Probanden. Dabei wies jeder Proband einen IgG (S1)-Wert > 384 BAU/ml und eine vergleichbare Neutralisationskapazität von >90 % gegenüber der Wildtyp- und Delta-Variante auf.
Material
1 ml Serum
Der Transport ins Labor ist nicht zeitkritisch und kann per Kurier oder Post erfolgen.
Abrechnung
Eine Abrechnung ist bisher nur im privatärztlichen Bereich (GOÄ) gegeben. Immunitätsuntersuchungen gehören bisher nicht zum Leistungsspektrum der GKVen. Selbstzahler entnehmen die Kosten bitte dem PDF-Dokument.
Literatur
- Addetia, A. et al. Neutralizing Antibodies Correlate with Protection from SARS-CoV-2 in Humans during a Fishery Vessel Outbreak with a High Attack Rate. JCM. Oct 2020, 58 (11)
- Tan, C.W. et al. A SARS-CoV-2 surrogate virus neutralization test based on antibody-mediated blockage of ACE2–spike protein–protein interaction. Nat Biotechnol 38, 1073–1078 (2020)
- Wu, J. et al. SARS-CoV-2 infection induces sustained humoral immune responses in convalescent patients following symptomatic COVID-19. medRxiv. 2020
- Sean C Taylor et al. A New SARS CoV-2 Dual Purpose Serology Test: Highly Accurate Infection Tracing and Neutralizing Antibody Response Detection. J Clin Microbiol 2021 26;JCM.02438-20. doi: 10.1128/JCM.02438-20.
- Hoffmann et al. The Omicron variant is highly resistant against antibodymediated neutralisation: Implications for control of the COVID-19 pandemic; Cell. 2022 Feb 3;185(3):447-456.e11.
- Jiahui Chen et al., Omicron Variant (B.1.1.529): Infectivity, Vaccine Breakthrough, and Antibody Resistance, J Chem Inf Model. 2022 Jan 24;62(2):412-422.