Nachweis von Soforttypallergien
Typ I-Allergien auf Acrylate und andere nicht-metallische Werkstoffe
Im Unterschied zu Metallen, wo allergische Unverträglichkeitsreaktionen ausschließlich auf lymphozytär vermittelte Typ IV-Sensibilisierungen zurückzuführen sind, können Immunreaktionen gegenüber acrylathaltigen Kompositmaterialien sowie auch anderen nicht-metallischen Werkstoffen auch IgE-vermittelt (Typ I-allergisch) sein.
An Soforttypallergien sollte gedacht werden, wenn die Symptomatik innerhalb wenigerStunden (selten sogar Minuten) nach Einbringung nicht-metallischer Zahnersatzmaterialien auftritt. Typisch sind lokale aber auch systemische ödematöse, quaddelartige Schleimhautaffektionen, wobei diese auf Grund der Besonderheiten der Schleimhäute lokal selten eine typische Morphe haben.
In der Literatur finden sich Hinweise, dass Patienten mit bekannten Soforttypallergien (Heuschnupfen, Insektengift- und Hausstauballergien) häufiger auch von einer Acrylatallergie betroffen sind, was auf eine prinzipielle Prädisposition für Typ I-Allergien hindeutet.
Wie erfolgt die Testung im Labor?
Für viele klassische Typ I-Allergene (z. B. Baumpollen) kann das spezifische IgE automatisiert in nahezu jedem Labor über EAST oder RAST-Verfahren bestimmt werden. Acrylate oder z.B. Inhalte von Wurzelfüllmaterialien sind allerdings bisher von keinem kommerziellen Anbieter etabliert worden. Die Diagnostik ist daher heute ausschließlich über zelluläre Testsysteme möglich.
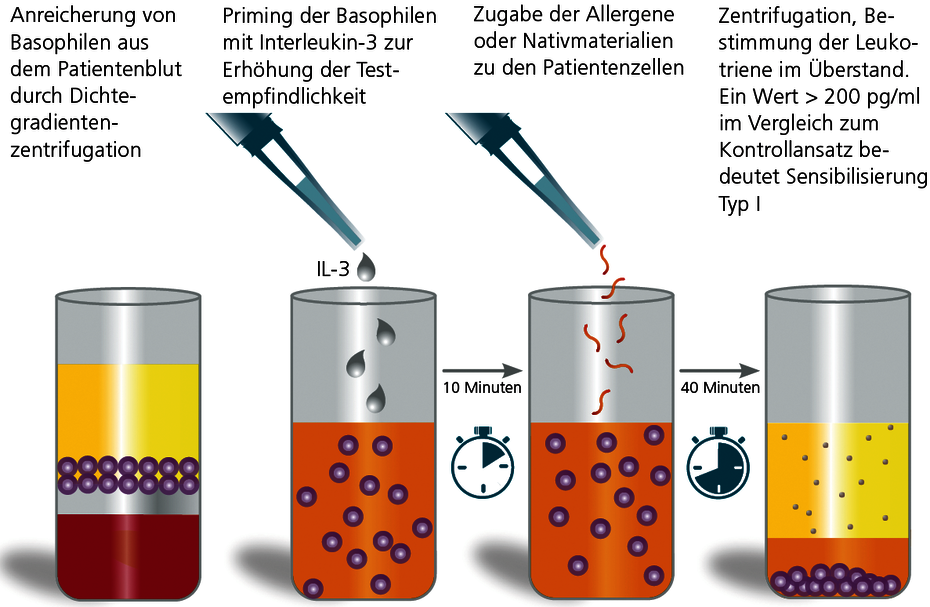
Der Basophilen-Degranulationstest (BDT) ist eine moderne in-vitro-Methode zum Nachweis Typ I-allergischer Sensibilisierungen sowie von Pseudoallergien. Der Test ist auch als Leukotrien-Release-Test, Basophilen-Aktivierungstest oder CAST-Test bekannt. Vorteil dieses Testes ist, dass sowohl Standardallergene (z.B. Acrylatmonomere) als auch native Materialproben nach Aufarbeitung im Labor getestet werden können. Dieses ermöglicht z.B. die Testung von Materialproben unbekannter Zusammensetzung (einschließlich von Prothesenmaterial oder in situ gewonnenen Kunststoffspänen).
Die Ergebnisse der Allergen-stimulierten Testansätze werden mit Positiv- und Negativkontrollen ins Verhältnis gesetzt. Ein resultierender Wert über 200 pg/ml bedeutet, dass eine Sensibilisierung vom Typ I vorliegt. Ein negatives Resultat schließt eine Sofort-Typ-Sensibilisierung mit hoher Sicherheit aus.
Hinsichtlich Sensitivität und Spezifität hat sich in unserem Labor der BDT gegenüber anderen in vitro-Provokationstesten wie Histamin-Freisetzungs-Test oder CD63-Test als eindeutig überlegen erwiesen.
Welche Zahnersatzmaterialien sind im BDT testbar?
Das Standard-Acrylat-Profil enthält:
Methylmethacrylat (MMA)
2-Hydroxyethylmethacrylat (HEMA)
Triethylenglycoldimethacrylat (TEGDMA)
Diurethandimethacrylat (DUDMA)
Alle weiteren gängigen Acrylate sind im Labor für die Testung vorrätig.
Auch Nativ-Proben können im BDT getestet werden.
Es ist allerdings auch möglich, eine Materialprobe (Kunststofftestplättchen, Proben von Wurzelfüllmaterialien, nativ gewonnene Späne, Zementproben o.ä.) mit ins Labor zu senden, auf welche dann direkt im BDT getestet wird. Das Material muss gemeinsam mit dem Blut eingesandt werden. Eine Reihe von Materialien sind im Labor auch vorrätig und für die Testung etabliert (siehe Rückseite des Anforderungsscheines Zahnmedizin). Vor allem bei Präventivtestungen sollten die Materialien in dem Zustand getestet werden, in dem sie später auch beim Patienten eingesetzt werden (z.B. ausgehärteter Kompositzement, auspolymerisierter Kunststoff).
Benötigtes Probenmaterial
2 ml EDTA-Blut oder Heparinblut pro Allergen bzw. Nativmaterial. Die Heparinmonovetten aus dem LTT-Abnahmeset können verwendet werden. Gerne senden wir Ihnen auch einzelne Abnahmeröhrchen zu. Ein Probeneingang im Labor innerhalb von 24h muss gewährleistet sein. Das Blut sollte bei Raumtemperatur gelagert und transportiert werden.
Abrechnung
Die Kosten betragen für Selbstzahler je Allergen 27,98 € (+ einmalig 23,31 € für die Zelltrennung). Für privatversicherte Patienten betragen die Kosten je Allergen 32,18 € (+ einmalig 26,81 € für die Zelltrennung). Privatkassen übernehmen bei gegebener Indikation die Kosten ohne Probleme.
Unverträglichkeit von Lokalanästhetika
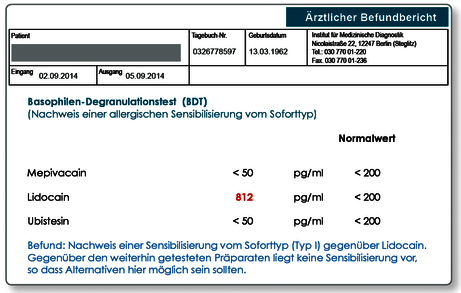
Überempfindlichkeiten auf Lokalanästhetika können allergischen Ursprungs sein.Vor allem wenn die Symptomatik innerhalb von Minuten bis wenigen Stunden eintritt, muss an IgE-vermittelte Sensibilisierungen oder Pseudoallergien gedacht werden. Anaphylaxien, d.h. systemische, zum Teil lebensgefährliche Überempfindlichkeitsreaktionen sind beschrieben. Bei Verdacht auf eine Unverträglichkeit auf Lokalanästhetika sollte eine Testung der Präparate im BDT erfolgen.
Im BDT sind prinzipiell alle Präparate einsetzbar, wenn eine Ampulle oder Tablette mit eingesandt wird. Folgende Wirkstoffe von Lokalanästhetika sind im Labor vorrätig und müssen deshalb nicht mit eingeschickt werden: Mepivacain, Articain, Lidocain, Prolocain und Ubistesin. Bei positiven Befunden wird ein Allergiepass ausgestellt. Ein positiv getestetes Präparat sollte prinzipiell nicht verwendet werden.
Benötigtes Probenmaterial
2 ml EDTA-Blut oder Heparinblut pro Präparat. Die Heparinmonovetten aus dem LTT-Abnahmeset können verwendet werden. Gerne senden wir Ihnen auch einzelne Abnahmeröhrchen zu. Ein Probeneingang im Labor innerhalb von 24h muss gewährleistet sein. Das Blut sollte bei Raumtemperatur gelagert und transportiert werden.
Abrechnung
Die Kosten betragen für Selbstzahler je Präparat 27,98 € (+ einmalig 23,31 € für die Zelltrennung). Für Privat versicherte Patienten betragen die Kosten je Präparat 32,18 € (+ einmalig 26,81 € für die Zelltrennung).
Literatur
- Kanerva L. Cross-reactions of multifunctional methacrylates and acrylates. Acta Odontol Scand. 2001;59:320-329.
- Lindström M, Alanko K, Keskinen H, Kanerva L. Dentist's occupational asthma, rhinoconjunctivitis, and allergic contact dermatitis from methacrylates. Allergy. 2002;57:543-545.
- Piirilä P, Hodgson U, Estlander T, Keskinen H, Saalo A, Voutilainen R, Kanerva L. Occupational respiratory hypersensitivity in dental personnel. Int Arch Occup Environ Health. 2002;75:209-216.
- Sanz ML, Gamboa P, de Weck AL. A new combined test with flowcytometric basophil activation and determination of sulfidoleukotrienes is useful for in vitro diagnosis of hypersensitivity to aspirin and other nonsteroidal anti-inflammatory drugs. Int Arch Allergy Immunol. 2005;136:58-72.
- de Weck AL, Sanz ML.Cellular allergen stimulation test (CAST) 2003, a review. J Investig Allergol Clin Immunol. 2004;14:253-273.