Autoantikörperdiagnostik von autoimmunen Lebererkrankungen
Bei chronischen Entzündungen der Leber oder Gallengänge (Hepatitis/Cholangitis) kann es sich auch um autoimmune Leberkrankungen handeln. Sie zeigen eine zunehmende Prävalenz und stellen eine Hauptursache für Leberzirrhose dar. Bei autoimmunen Lebererkrankungen kommt es zum Verlust der Selbsttoleranz gegenüber dem hepatozellulären oder cholangiozellulären Gewebe. Ursächlich dafür sind am ehesten eine Kombination aus verschiedenen Umweltfaktoren (z. B. Infektionen, Umwelttoxine, Medikamente) und einer genetischen Prädisposition. Prinzipiell kann man drei Krankheitsbilder unterscheiden:
- die autoimmune Hepatitis (AIH)
- die primär biliäre Cholangitis (PBC)
- die primär sklerosierende Cholangitis (PSC)
Neben diesen Haupterkrankungen sind einige Overlap-Syndrome, insbesondere zwischen der AIH und PBC bekannt. Die Prävalenz der AIH beträgt ca. 10 - 30/100.000 Einwohner, die der PBC etwa 30 - 40/100.000 Einwohner, wobei bei beiden Erkrankungen bevorzugt das weibliche Geschlecht betroffen ist. Die Prävalenz der PSC wird mit bis zu 16/100.000 Einwohner angegeben.
1. Autoimmunhepatitis (AIH)
Die AIH wird aktuell international gebräuchlich aufgrund serologischer Kriterien (Autoantikörper) und des Manifestationsalters in 2 verschiedene Subformen eingeteilt (Tabelle 1). Die klassische AIH (Typ 1) ist durch den Nachweis von anti-nukleären Antikörpern (ANA) und/oder Autoantikörpern (AAk) gegen die glatte Muskulatur (smooth muscle antibodies, ASMA, SMA) gekennzeichnet. Auch die AIH, die mit AAk gegen SLA (soluble liver antigen/liver pancreas antigen) assoziiert ist, wird nun als Typ 1-Variante betrachtet. Hiervon abzugrenzen ist eine zweite Verlaufsform (AIH Typ 2), die durch LKM-1-AAk (liver-kidney microsomal antibodies) und/ oder LC-1-AAk (liver-cytosolic antibodies) charakterisiert ist.
| Typ 1- AIH | Typ 2- AIH | |
|---|---|---|
| Häufigkeit | ca. 90 % der AIH-Fälle | ca. 10 % der AIH-Fälle |
| Manifestationsalter | 10-25 & 45-70 Jahre | < 15 Jahre |
| Prognose | gutes Therapieansprechen | Prognose ungünstiger |
| Autoantikörper | ANA, ASMA, SLA-AAk | LKM1-AAk, LC1-AAk |
Tabelle 1 Serologische Klassifikation der Autoimmunhepatitis
ANA
Ca. 50 % der Patienten mit AIH sind ANA-positiv. Obwohl sie keine Spezifität für die AIH besitzen, zählen sie zu den Klassifikationskriterien der AIH. Sie gelten als Markerantikörper und entsprechend der International Autoimmune Hepatitis Group als Diagnosekriterium AIH Typ 1. ANA und ASMA finden sich bei bis zu 80 % der Patienten mit AIH, wobei ca. 15 % isoliert ANA besitzen.
ASMA
Hohe Titer von ASMA gelten als Markerantikörper und entsprechend der International Autoimmune Hepatitis Group als Diagnosekriterium der AIH Typ 1. Sie sind sehr häufig mit ANA assoziiert, kommen jedoch auch in ca. 35 % der Fälle isoliert vor. Ein negativer ASMA-Befund schließt eine AIH nicht vollständig aus. Die Titer korrelieren eingeschränkt mit der Krankheitsaktivität. Meist niedrige Titer werden bei Virusinfektionen, wie infektiöser Mononukleose, chronischer Hepatitis C (8-10 %), aber auch bei Erkrankungen des rheumatischen Formenkreises, bei PBC (22 %), bei alkohol-induzierten Leberschäden (3-16 %) und neoplastischen Erkrankungen gefunden. Die Prävalenz bei Gesunden beträgt ca. 5 % . Als relevantes Zielantigen für die AIH- Diagnostik wurde F-Aktin identifiziert.
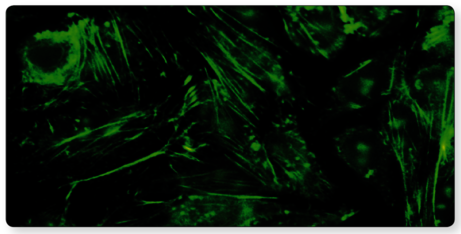
Abb. 1 Nachweis von ASMA mittels indirekter Immunfluoreszenztechnik (IFT): ASMA vom Typ Aktin binden an Aktinfilamente im Zytoskelett einer Zelle und zeigen das typische fibrilläre Fluoreszenzmuster (Fa. Euroimmun).
SLA/LP-AAk
SLA/LP-Antikörper haben unter allen AAk die höchste Spezifität für die AIH. Sie sind jedoch nur bei etwa 10 bis 20 % der Patienten nachweisbar und der prädiktive Wert beträgt nahezu 100 %. SLA/LP-AAk finden sich isoliert (ca. 10 %), meistens jedoch in Kombination mit ANA und ASMA. SLA/LP-AAk wurden bei Virushepatitiden nicht nachgewiesen.
LKM-1-AAk
LKM-1-Antikörper sind Markerantikörper und entsprechend der International Hepatitis Group ein Diagnosekriterium der AIH Typ 2 mit einer Sensitivität von 90-95 % bei (vorzugsweise) jungen Patienten. Gelegentlich werden LKM-1-AAk bei Patienten mit einer chronischen Hepatitis C-Virusinfektion gefunden (6 -10 %).
LC-1-AAk
LC-1-Antikörper gelten als zweiter Markerantikörper der AIH Typ 2 und sind hauptsächlich bei jungen Patienten nachweisbar. Sie kommen meistens gleichzeitig mit LKM-1-AAk vor, treten aber auch bei einem Drittel der AIH-2-Patienten isoliert auf. LC-1-AAk gelten als weitgehend spezifisch für die AIH Typ 2, wenngleich sie auch in seltenen Fällen bei chronischer Hepatitis C oder AIH Typ 1 nachweisbar sind.
Die Diagnosesicherung erfordert den Ausschluss anderer Faktoren, die eine Hepatitis verursachen können, wie z. B. virale Hepatitiden. Hilfreich ist der vereinfachte AIH-Score (Hennes EM et al. Hepatology 2008) (Tabelle 2), der auf einem Punktesystem basiert. Für die AAk können maximal 2 Punkte vergeben werden, auch wenn mehrere AAk nachweisbar sind. Beweisend ist der gemeinsame Nachweis von AAk und eine Erhöhung der γ-Globuline bei gleichzeitigem Ausschluss einer viralen Genese. Bei einem Score ≥ 6 ist eine AIH wahrscheinlich, bei einem Score ≥ 7 gilt sie als gesichert.
| Parameter | Wertungskriterium | Punkte |
|---|---|---|
| ANA oder ASMA | Titer ≥1:40 Titer ≥1:80 | 1 2 |
| LKM-AAk | Titer ≥1:40 | 2 |
| SLA/LP-AAk | Positiv | 2 |
| Gesamt-IgG | > Normwert > 1,1-facher Normwert | 1 2 |
| Leberhistologie | Atypisch Passend zu AIH AIH-typisch | 0 1 2 |
| Ausschluss Virushepatitis | Nein Ja | 0 2 |
Tabelle 2 Vereinfachter Autoimmunhepatitis-Score nach Hennes et al. (2008)
2. Primär biliäre Cholangitis (PBC)
Die PBC ist eine chronisch-cholestatische Lebererkrankung, die mit Entzündung und Fibrose der Leber einhergeht und hauptsächlich bei Frauen mittleren Alters auftritt. Ohne rechtzeitige Diagnose und adäquate Behandlung kann sich im Verlauf der Erkrankung eine Leberzirrhose entwickeln. Oftmals ist die PBC mit anderen Autoimmunerkrankungen, wie z. B. Sjögren-Syndrom, Hashimoto-Thyreoiditis, rheumatoider Arthritis oder Zöliakie assoziiert. Diagnostisch wegweisend sind spezifische und frühe Marker-Autoantikörper, zu denen die AMA (M2-AMA) und bestimmte ANA-Typen gehören.
AMA (anti-mitochondriale Antikörper)
AMA gelten als Markerantikörper und zählen zu den drei Diagnosekriterien einer primär biliären Cholangitis (PBC) und sind in ca. 95 % der Fälle nachweisbar. Sie sind vorzugsweise gegen das M2-Antigen gerichtet. Die in der Immunfluoreszenztechnik (IFT) zu beobachtenden AMA sind nicht alle mit der PBC assoziiert. Deshalb sollte einem positiven AMA-IFT-Ergebnis die Bestimmung der hochspezifischen M2-AMA folgen. Allerdings sind M2-AMA auch gelegentlich bei Patienten mit chronischen entzündlich-rheumatischen Erkrankungen nachweisbar. Es wird angenommen, dass diese Patienten ein erhöhtes Risiko haben, zusätzlich zu der Grunderkrankung eine PBC zu entwickeln. AMA besitzen eine prädiktive Bedeutung, da sie der PBC-Manifestation um viele Jahre vorausgehen können.
ANA
- Fluoreszenzmuster „mehrere nukleäre Punkte”
Diesem ANA-Fluoreszenzmuster liegt das Hauptantigen Sp100 zugrunde. Autoantikörper gegen Sp100 gelten als spezifisch (97 %) für die PBC und sind in 20 - 40 % der Fälle von Patienten mit einer PBC nachweisbar. Relativ häufig (48 %) findet man diese AAk in der Gruppe der AMA-negativen Patienten mit einer klinisch und histologisch gesicherten PBC. Damit stellen die Sp100-AAk eine wesentliche Ergänzung der AMA dar. Der gleichzeitige Nachweis von AMA und Sp100-AAk gilt als hochspezifisch für die PBC. Bei AIH oder primär sklerosierender Cholangitis (PSC) sind Sp100- AAk nicht oder nur sehr selten nachweisbar. In geringer Frequenz werden die Sp100-AAk bei Erkrankungen des rheumatischen Formenkreises (z. B. Rheumatoide Arthritis oder SLE) gefunden. - Fluoreszenzmuster „nukleär randständig (Kernmembran)“
Dieses ANA-Fluoreszenzmuster kann durch Autoantikörper gegen gp210 hervorgerufen werden. gp210-AAk gelten als hochspezifisch für eine PBC und sind in bis zu 45 % der Fälle von Patienten mit PBC nachweisbar. In 21 - 47 % der Fälle findet man gp210-AAk bei einer AMA-negativen klinisch gesicherten PBC. Ihre Spezifität beträgt 99,5 %; sie sind sehr selten bei AIH, rheumatoider Arthritis, Polymyositis oder Sjögren-Syndrom zu beobachten. gp210-AAk sind mit extrahepatischen Manifestationen, wie Arthritis, assoziiert. Sie gelten als Prognosemarker und weisen auf einen ungünstigen Verlauf der PBC hin. - Fluoreszenzmuster „Zentromere“
Einige Patienten mit histologisch gesicherter PBC weisen ausschließlich AAk gegen Zentromere auf. Diese gelten als diagnostische Marker der systemischen Sklerodermie, sind jedoch auch in 10-30% der Fälle bei Patienten mit PBC nachweisbar. Zentromer-AAk zeigen einen eher prognostisch ungünstigen Verlauf an und können auf eine assoziierte Sklerodermie oder eine mögliche Sklerodermie-Entwicklung hinweisen.
3. Primär sklerosierende Cholangitis (PSC)
Während die AIH und PBC durch typische AAk-Befunde charakterisiert sind, sind bei der PSC keine krankheitsspezifischen AAk bekannt. Die größte Bedeutung kommt den pANCA und aANCA (atypische ANCA) zu, die häufig (bis zu 80 %) bei PSC-Patienten gefunden werden, aber keine beweisenden diagnostischen Marker der PSC sind, da sie als Marker-AAk der ANCA-assoziierten Vaskulitiden gelten. Im Gegensatz zu den pANCA bei Vaskulitiden reagieren diese ANCA allerdings nicht mit dem Autoantigen MPO (Myeloperoxidase).
Material
1 ml Serum
Der Transport ins Labor ist nicht zeitkritisch und kann per Postversand erfolgen.
Abrechnung
Die Abrechnung im kassen- und privatärztlichen Bereich ist gegeben.
Literatur
- Strassburg CP et al. S2k Leitlinie autoimmune Lebererkrankungen. Z Gastroenterol 2017
- Conrad, Schößler, Hiepe. Autoantibodies in Organ Specific Autoimmune Diseases. A Diagnostic Reference. Pabst Science Publishers 2017
- Fischer HP et al. Der Pathologe 2020
- Hennes EM et al. Hepatology 2008)
- Schultheiß C et al. B cells in autoimmune hepatitis: bystanders or centralplayers? Semin Immunopathol 2022
- Sebode M et al. Autoantibodies in autoimmune liver disease—clinical and diagnostic relevance. Front Immunol 2018
- Lohse et al. Update S3-Leitlinie LeiSe LebEr – autoimmune Lebererkrankungen. 2025