Lektin reaktives α-Fetoprotein (AFP-L3) und des-Gamma-Carboxy Prothrombin (DCP)
Neue Marker zur Überwachung des hepatocellulären Carcinoms (HCC) sowie zur verbesserten Wahrscheinlichkeit der Früherkennung
In Deutschland erkranken pro Jahr ca. 6.000 Menschen an einem HCC, wobei ca. 70% der Patienten erst in einem fortgeschrittenen Stadium diagnostiziert werden. Das HCC ist der fünfthäufigste Tumor weltweit mit einer ansteigenden Inzidenz. Zu den Risikofaktoren zählen an erster Stelle chronischer Alkoholabusus sowie chronische Hepatitiden durch HCV- und HBV-Infektionen. Aber auch die seltene erbliche Stoffwechselerkrankung Tyrosinämie Typ I (Hepatorenale Tyrosinämie) ist mit einer erhöhten Rate an HCC assoziiert. Ca. 1/3 der Patienten entwickelt ein HCC in Folge einer Leberzirrhose.
Wie bei anderen bösartigen Tumorerkrankungen ist eine frühzeitige Erkennung der entscheidende Faktor, um Patienten einen kurativen Therapieansatz zu ermöglichen. In der aktuellen gemeinsamen Leitlinie der Europäischen Gesellschaft zum Studium der Leber (EASL) und der Organisation für Studien zur Krebstherapie (EORTEC) wird die Überwachung von HCC-Risikopatienten durch abdominelle Sonographie in sechsmonatigen Intervallen empfohlen. Insbesondere bei den fortgeschrittenen Zirrhosestadien ist die sonographische Beurteilung des Leberparenchyms erschwert. In einer Studie aus den USA wird deshalb neben der Sonographie auch die AFP-Bestimmung empfohlen, weil sich so die Sensitivität der HCC- Erkennung gegenüber der alleinigen Sonographie signifikant erhöht.
AFP-L3 ist eine HCC-spezifische Isoform des in der Leber gebildeten α-Fetoproteins mit zusätzlicher α-1-6-Fukoseeinheit am reduzierenden Ende eines N-Acetylglukosamins. An dieser Modifikation bindet das Lektin Lens Culinaris Agglutinin (LCA). AFP-L3% stellt das prozentuale Verhältnis des AFP-L3 zum Gesamt AFP dar.
DCP, des-Gamma-Carboxy Prothrombin, ist eine Vorstufe des Prothrombins. Während des normalen Stoffwechsels unterliegt DCP einer Vitamin-K-abhängigen Carboxylierung von zehn Glutaminsäureresten am N-Terminus (γ-Carboxylierung). Im Falle eines HCC kann diese Reaktion gestört sein, so dass sich DCP im Blutplasma anreichert. DCP ist in der Literatur auch als „protein induced by vitamin K absence oder Antagonist II“ (PIVKA-II) bekannt.
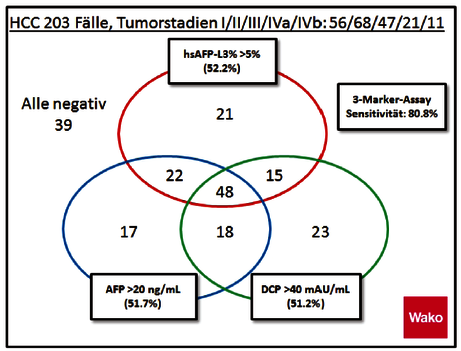
Quelle: Sapporo Kousei Krankenhaus
Vorteile der neuen Parameter
Wie die Abbildung 1 veranschaulicht, ermöglichen die Bestimmungen von AFP-L3 und DCP zusätzlich zu AFP eine erhöhte Detektionsrate von HCCPatienten. So wurden durch den gleichzeitigen Einsatz beider Marker 78% einer HCC-Patientengruppe mit AFP-Werten unter 10 ng/ml mit einer Spezifität von 86% detektiert. AFP-Werte von 10 ng/ml liegen bei der im IMD Berlin-Potsdam verwendeten Methode im Grauzonenbereich. Hier liegt eine wesentliche Verbesserung der möglichen Früherkennung eines HCC.
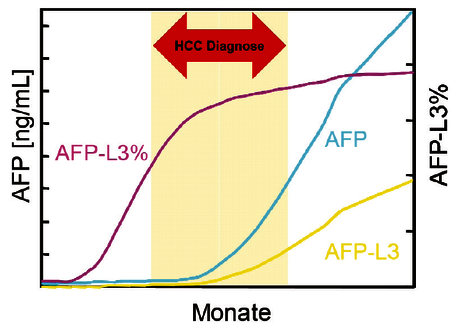
Bei anderer Betrachtungsweise spiegelt die gleichzeitige Bestimmung der Parameter AFP, AFP-L3 % und DCP einen sehr hohen negativen Vorhersagewert von 91% wider9.
Methodik
Sowohl AFP-L3 als auch DCP werden auf einer neuartigen Plattform mittels Kapillarelektrophorese in mikrofluidischen Analysenchips aufgetrennt und gemessen.
Diagnostisches Vorgehen
Wir empfehlen entsprechend den hier vorgestellten Daten ein laborseitiges Triple-Screening bestehend aus AFP, AFP-L3 und DCP bei entsprechenden Risikopatienten ergänzend zu der von der EORTEC vorgeschlagenen Lebersonographie.
Probenmaterial
Serum (Vollblutmonovette)
Eine besondere Patientenvorbereitung ist nicht erforderlich. Ein Vitamin-K-Mangel sollte vor der Bestimmung von DCP ausgeschlossen sein.
Abrechnung
PKV Patienten: erstattungsfähig. Bitte entnehmen Sie die Untersuchungskosten dem PDF-Dokument.
GKV Patienten: Erstattungsfähig bei begründeter medizinischer Notwendigkeit. Hier muss auf dem Überweisungsformular angegeben werden: „Verdacht auf HCC, Hochrisikopatient mit Leberfibrose!“.
Literatur
- Robert Koch Institut (Hrsg.): Krebs in Deutschland 2007/2008. Häufigkeiten und Trends, Berlin 2012
- EASL-EORTC Clinical Practice Guidelines. Management of hepatocellular carcinoma. Journal of Hepatology 2012 (56): 908-943
- Singal AG et al. Effectiveness of hepatocellular carcinoma surveillance in patients with cirrhosis. Cancer Epidemiol Biomarkers Prev. 2012 (30)
- Kagebayashi C et al. Automated immunoassay system for AFP-L3 using on-chip elektrokinetic reaction and separation by affinity electrophoresis. Anal Biochem 2009,15:388 (2):306-11
- Arii S. et al. Management of hepatocellular carcinoma. Report of Consensus Meeting in the 45th Annual Meeting of the Japan Society of Hepatology (2009). Hepatol Res. 2010;40:667-85
- Toyoda H. et al. Prognostic significance of simultaneous measurement of three tumor markers in patients with hepatocellular carcinoma. Clin Gastroenterol Hepatol. 2006;4:111-7
- Hanaoka et al. Clinical significance of the highly sensitive fucosylated fraction of α-fetoprotein in patients with chronic liver disease. J Gastroenterol Hepatol. 2011;26(4):739-44
- Toyoda H. et al. Clinical utility of highly sensitivity Lens Culinaris agglutinin-reactive alpha-fetoprotein in hepatocellular carcinoma patients with alpha-fetoprotein < 20 ng/ml. Cancer Sci. 2011;102(5):1025-31
- Carr BI, Kanke F, Wise M, Satomura S Clinical Evaluation of lens culinaris agglutinin reactive a-fetoproteinand des-gamma carboxy prothrombin in histologicallyproven hepatocellular carcinoma. J. Surg Oncology 2012; 102:462-8




