Paroxysmale nächtliche Hämoglobinurie (PNH)
Klinische Bedeutung und Symptome
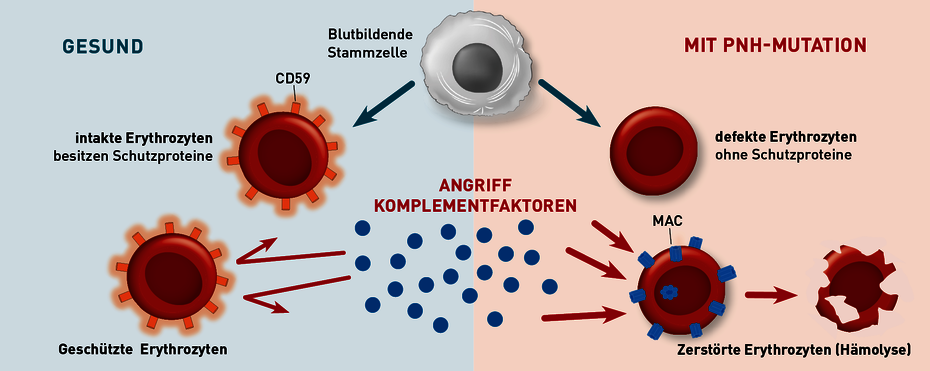
Die paroxysmale nächtliche Hämoglobinurie (PNH) ist eine erworbene Erkrankung der Blutstammzellen. Durch eine erworbene Mutation im Gen PIG-A kommt es zu einer verminderten Bildung von Glykosyl-Phosphatidylinositol- (GPI-) Ankern. Diese GPI-Anker werden benötigt, um bestimmte Moleküle auf der Zellmembran zu verankern. Unter anderem sind Proteine, die die Zellen vor einem Angriff des Komplementsystems schützen, solche GPI-verankerten Moleküle. Die Mutation tritt zufällig in einzelnen Blutstammzellen auf und alle aus dieser Zelle hervorgehenden Tochterzellen tragen dann auch die Mutation. Der fehlende Schutz vor dem Komplementsystem führt zu einer Zerstörung der Erythrozyten, also zu einer Hämolyse (siehe Abb. 1). Die dadurch verursachte Freisetzung von Hämoglobin und die Depletion von NO (Stickstoffmonoxid) ist der Grund für die Symptome sowie die Mortalität der PNH.
Die PNH ist eine sehr seltene Erkrankung, die in einer Häufigkeit von 16 Fällen auf 1 Million Menschen vorkommt. Durch eine Hemmung des Komplementsystems kann sie seit einigen Jahren effektiv behandelt werden. Unbehandelt beträgt die Lebenserwartung ca. 10 Jahre; mit den modernen Therapien kann eine normale Lebenserwartung erreicht werden.
Nur selten fällt die PNH über die oft als klassisches Zeichen angesehene Ausscheidung von Hämoglobin über den Urin auf. Viel häufiger sind unspezifische Symptome. Fast alle Patienten klagen über eine ausgeprägte Fatigue. In absteigender Häufigkeit leiden die Patienten an einer Anämie, Atemnot, chronischer Niereninsuffizienz, Bauchschmerzen, pulmonaler Hypertonie, erektiler Dysfunktion oder Schluckbeschwerden. 40 % der Patienten erleiden eine Thrombose und nur 25 % haben das klassische Bild einer Hämoglobinurie.
Diagnostik der PNH
Die Diagnostik einer PNH erfolgt mittels Durchflusszytometrie. Hierzu wird die fehlende Expression von GPI-verankerten Molekülen auf Erythrozyten und Leukozyten nachgewiesen. Die kürzlich überarbeiteten internationalen Leitlinien zur PNH-Diagnostik empfehlen die Verwendung sehr sensitiver Methoden, die auch den Nachweis geringster Anteile GPI-defizienter Zellen erlauben (0,01 % für Erythrozyten und 0,1 % für Leukozyten). Dies ist insbesondere für die bei einer aplastischen Anämie vorkommenden PNH-Klone sehr wichtig, da diese mit den älteren Methoden oft nicht detektiert werden können.
Weil die PNH so selten ist, sollten beim Vorliegen von Hämolysezeichen (erhöhte LDH und/oder vermindertes Haptoglobin und/oder erhöhte Retikulozyten) zunächst andere Ursachen ausgeschlossen werden.
In folgenden Fällen besteht jedoch eine klare Indikation für eine PNH-Testung:
- unerklärte Zytopenie in Kombination mit Hämolysezeichen
- unerklärte und atypische Thrombose (trotz Antikoagulation, bei Pat. < 50 Jahre, ungewöhnliche Lokalisation (Budd-Chiari-Syndrom, zerebral, mesenterial, dermal oder subclaviculär)) in Kombination mit Hämolysezeichen
- Hämolytische Anämie mit negativem Coombs-Test
- Unerklärte Hämoglobinurie
- Patienten mit Aplastischer Anämie
- Patienten mit Myelodysplastischem Syndrom (insbesondere Fälle mit niedrigem Risiko)
- Erwogen werden sollte eine PNH-Testung bei Patienten mit einer Fatigue in Kombination mit Hämolysezeichen.
Abb. 1 Pathophysiologie der PNH: Links dargestellt sind Erythrozyten mit normaler Expression des Moleküls CD59, das vor dem Angriff des Komplementsystems schützt. Rechts Erythrozyten mit Verlust der CD59-Expression. Hier kommt es zu einer Aktivierung des Komplementsystems mit Bildung des Membran-AngriffsKomplexes (MAC) und darauf folgender Zerstörung der Zellen.
Erläuterung des Befundes
Auch die Darstellung und Interpretation des Befundes erfolgt nach den im Jahr 2018 aktualisierten Richtlinien. Für die Erythrozyten geben wir jeweils den Anteil der Zellen ohne (Typ-I-Zellen), mit partiellem (Typ-II-Zellen) und vollständigem Verlust (Typ-III-Zellen) der Expression des GPIverankerten Moleküls CD59 an. Die Summe aus Typ-II- und Typ-III-Zellen ergibt dann die Gesamtgröße der GPI-defizienten Erythrozytenpopulation. Für die Leukozyten erfolgt die Darstellung getrennt nach Monozyten und Neutrophilen Granulozyten. Auf diesen Zellen werden jeweils drei GPIverankerte Moleküle untersucht. Eine Unterteilung in Zellen mit partiellem oder vollständigem Markerverlust ist für diese Zellen nicht sinnvoll. Für jede Population wird zusätzlich die untere Grenze des Messbereichs angegeben. So ist im Befund nachvollziehbar, mit welcher Sensitivität der Ausschluss von GPI-defizienten Zellen erfolgte.
Neben diesen numerischen Angaben enthält der Befund selbstverständlich auch Hinweise zur Interpretation des Ergebnisses sowie Empfehlungen zu Folge- und Wiederholungsuntersuchungen. Damit folgen wir den internationalen Bemühungen zu einer verbesserten Standardisierung der PNH-Diagnostik, was vor dem Hintergrund der Seltenheit dieser Erkrankung notwendig erscheint.


Material
Die Bestimmung erfolgt aus EDTA-Blut (mindestens 1 ml). Die Probe sollte innerhalb von 24 Stunden im Labor sein.
Abrechnung
Die Untersuchung wird von der GKV (auf Überweisung Muster 10) und der PKV übernommen.
Literatur
- Dezern AE, Borowitz MJ. ICCS/ESCCA consensus guidelines to detect GPI-deficient cells in paroxysmal nocturnal hemoglobinuria (PNH) and related disorders part 1 - clinical utility. Cytometry B Clin Cytom. 2018 Jan;94(1):16-22.
- Sutherland DR, Illingworth A, et al. ICCS/ESCCA consensus guidelines to detect GPI-deficient cells in paroxysmal nocturnal hemoglobinuria (PNH) and related disorders part 2 - reagent selection and assay optimization for high-sensitivity testing. Cytometry B Clin Cytom. 2018 Jan;94(1):23-48.
- Illingworth A, Marinov I, et al.ICCS/ESCCA consensus guidelines to detect GPI-deficient cells in paroxysmal nocturnal hemoglobinuria (PNH) and related disorders part 3 - data analysis, reporting and case studies. Cytometry B Clin Cytom. 2018 Jan;94(1):49-66.
- Oldaker T, Whitby L, Saber M, et al. ICCS/ESCCA consensus guidelines to detect GPI-deficient cells in paroxysmal nocturnal hemoglobinuria (PNH) and related disorders part 4 - assay validation and quality assurance. Cytometry B Clin Cytom. 2018 Jan;94(1):67-81.