Genetik der Medikamentenverstoffwechselung (Pharmakogenetik)
Ungünstige genetische Ausstattungen des Entgiftungssystems können nicht nur unerwünschte Arzneimittelwirkungen hervorrufen, sondern auch die Entwicklung verschiedener Erkrankungen fördern. Dazu gehören Migräne, chronisches Erschöpfungssyndrom (CFS), multiple Chemikalien-Sensitivität (MCS), Tumore, Rheuma, Alzheimer und andere chronische Erkrankungen.
Biochemie
Bedingt durch fortschreitende Entwicklungen der chemischen und pharmazeutischen Industrie, aber auch höhere Belastung der Umwelt ist der menschliche Organismus einer immer größer werdenden Menge an Schadstoffen, Fremdstoffen und Medikamenten ausgesetzt. Diese müssen vom Entgiftungssystem des Körpers (vor allem der Leber) metabolisiert werden. Die exogenen Fremdstoffe sind meist lipophil, so dass sie ohne weitere Modifikation nicht ausgeschieden werden können. Dies gilt auch für viele endogen synthetisierte Stoffe, wie z.B. Hormone. Dem menschlichen Organismus steht für den Metabolismus dieser Substanzen eine spezifische Enzymausstattung zur Verfügung, die die Neutralisierung und somit die Umwandlung in ausscheidungsfähige Endprodukte ermöglicht.
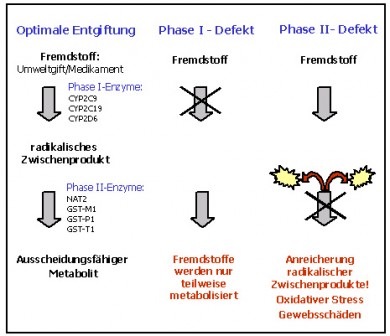
Dieser Detoxifikationsprozess läuft in zwei Phasen ab:
Verminderter Phase I-Metabolismus führt zu verminderter Entgiftung der Ausgangsprodukte. Eine reduzierte Phase II-Entgiftung hat dagegen die Anreicherung radikaler oder toxischer Intermediärprodukte zur Folge.
In der ersten Phase werden toxische Substanzen mittels verschiedener Cytochrom P450-Enzyme reduziert, hydrolysiert und oxidiert. Die Produkte der Phase I sind zumeist kurzfristig sogar aggressiver als das primäre Toxin, so dass die schnelle Entgiftung in der Phase II essentiell ist.
In der zweiten Phase werden dann polare hydrophile Moleküle wie Glutathion, Acetat, Cystein, Sulfat, Glycin oder Glucuronat an die Metaboliten der Phase I angelagert.
Erst jetzt stehen diese in wasserlöslicher Form für die biliäre bzw. renale Ausscheidung zur Verfügung. Wichtige Phase-II-Enzyme sind: Glutathion-S-Transferasen (GST) und N-Acetyltransferasen (NAT).
Diagnostik
Die Effektivität der Metabolisierung von Arzneimitteln und Fremdstoffen ist von einem optimalen Zusammenspiel der am Entgiftungsprozess beteiligten Enzyme abhängig. Genetische Polymorphismen in den Enzymen des Arzneimittelstoffwechsels können zu unerwünschten Nebenwirkungen führen oder für eine fehlende therapeutische Wirkung verantwortlich sein.
Phase I
Genvarianten in den Cytochrom P450 (CYP)-Enzymen CYP1A1, CYP1A2, CYP2A6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 und CYP3A5 geben Auskunft darüber, ob bestimmte Gruppen von Schadstoffen entgiftet werden können oder sich im Körper anreichern.
Phase II
Genvarianten in den Glutathion-S-Transferasen (GST) GST-M1, GST-T1 und GST-P1 führen zu einer schlechteren Entsorgung der äußerst radikalen Zwischenprodukte aus den Phase I-Reaktionen und vermitteln dadurch eine Disposition für Tumore, neurodegenerative Erkrankungen und Zustände, die mit oxidativem Stress assoziiert sind. Ausbleibende therapeutische Wirkungen von Medikamenten gehen damit ebenfalls einher.
Varianten im N-Acetyltransferase 2 (NAT2)-Gen führen in der Phase II zum „langsamen Acetylierer“-Typ. Durch Anreicherung toxischer Phase I-Metabolite kann es zu klinisch relevanten unerwünschten medikamentösen Nebenwirkungen, wie Hypersensitivität, Neuropathie oder Leukopenie kommen.
Chemotherapeutika
Eine Thiopurin-S-Methyltransferase (TPMT)-Defizienz führt zur hämatopoetischen Toxizität mit Myelosuppression nach Gabe von Azathioprin, 6-Mercaptopurin oder 6-Thioguanin. Die Häufigkeit von homozygoter TPMT-Defizienz bei Kaukasiern wird mit etwa 1:300 angegeben. Die heterozygote TPMT-Defizienz findet man bei 10% der Bevölkerung. Auch diese Gruppe hat ein größeres Risiko für Nebenwirkungen infolge der Einnahme thiopurinhaltiger Arzneimittel.
Bei der Chemotherapie mit 5-Fluorouracil (5-FU) und dessen Prodrug (Capecitabin) ist die Funktionalität der Dihydropyrimidin-Dehydrogenase (DPD) als wichtigstes Abbauenzym von entscheidender Bedeutung. Varianten im DPD-Gen führen zu einem verringerten Metabolismus und können zu unerwünschten toxischen Reaktionen führen (z.B. Myelosuppression).
Patienten, die eine genetisch bedingt veränderte Aktivität des Enzyms Methylentetrahydrofolat-Reduktase (MTHFR) aufweisen, haben unter Therapie mit Methotrexat ein erhöhtes Risiko für das Auftreten von Nebenwirkungen (z.B. schwere Blutbildveränderungen, Mukositis, Hyperhomocysteinämie).
Transportproteine
Das Multidrug resistance-1 (MDR1)-Gen kodiert für das Transportmolekül P-Glycoprotein (PGP), über das zahlreiche Medikamente aus der Zelle geschleust werden. Ein Polymorphismus im MDR-1-Gen führt zur erniedrigten Aktivität des Transporters und somit zu einer höheren Resorption und Bioverfügbarkeit der betroffenen Pharmaka.
Indikationen
- In Vorbereitung entsprechender medikamentöser Therapien bzw. bei Verdacht auf Arzneimittelunverträglichkeiten
- Patienten mit Verdacht auf umweltmedizinische Erkrankungen durch berufliche oder anderweitige Schadstoffexposition
- präventiv bei Personen mit permanenter beruflicher Schadstoffexposition (insbesondere Kanzerogene)
Probenmaterial und Anforderung
2 ml EDTA-Blut
Der Transport ins Labor ist nicht zeitkritisch und kann per Postversand erfolgen. Bei genetischen Untersuchungen ist eine Einwilligungserklärung erforderlich. Ein entsprechendes Formular stellen wir Ihnen gern zur Verfügung.
Abrechnung
Pharmakogenetische Untersuchungen werden von privaten und bei einigen Indikationen (siehe Anforderungsschein Pharmakogenetik) auch von gesetzlichen Kassen getragen. Als eine molekulargenetische Untersuchung ist die Anforderung Laborbudget-befreit. (Ziffer 32010). Toxikogenetische Untersuchungen werden von privaten Kassen erstattet. Kassenversicherte können diese Leistungen als Selbstzahler anfordern.
Wichtige Enzyme für die Metabolisierung von Arzneimitteln bzw. deren Substraten sind in der folgenden Tabelle aufgeführt. Die Auswahl ist beispielhaft:
| Alprenolol | CYP2D6 | Moclobemid | CYP2C19, CYP2D6 |
| Amiodaron | CYP3A4 | Modafinil | CYP2C19 |
| Amitriptylin | CYP2C19, CYP2D6 | Morphin | CYP2D6 |
| Amphetamine | CYP2D6 | Naproxen | CYP1A2 |
| Anthracycline | MDR1 | Nitrazepam | NAT2 |
| Barbiturate | CYP2C19 | Nortriptylin | CYP2D6 |
| Bufuralol | CYP2D6 | Omeprazol | CYP2C19, CYP2D6 |
| Caffeine | CYP1A1, CYP1A2 | Paclitaxel (Taxane) | MDR1 |
| Captopril | CYP2D6 | Pantoprazol | CYP2C19 |
| Carbamazepin | CYP2C19 | Paroxetin | CYP2D6 |
| Carvedilol | CYP2D6 | Perphenazin | CYP2D6 |
| Celecoxib | CYP2C9 | Phenobarbital | CYP2C19 |
| Chinidin | CYP2D6 | Phenylbutazon | CYP2C19, CYP2C9 |
| Chlorpropamid | CYP2D6 | Phenytoin | CYP2C19, CYP2D6 |
| Cimetidin | CYP2D6 | Piroxicam | CYP2C9 |
| Citalopram | CYP2C19, Cyp3A4 | Prednisolon | CYP2C19 |
| Clomipramin | CYP2C19, CYP2D6 | Procainamid | NAT2 |
| Clonazepam | NAT2 | Proguanil | CYP2C19 |
| Clozapin | CYP1A1, CYP1A2 | Propafenon | CYP2D6 |
| Cocain | CYP2D6 | Propranolol | CYP1A2, CYP2C19, CYP2D6 |
| Codein | CYP2D6 | Ranitidin | CYP2D6 |
| Coumaid | CYP2C9 | Remoxiprid | CYP2D6 |
| Cyclosporin A | CYP3A4, CYP3A5 | Risperidon | CYP2D6 |
| Desipramin | CYP2D6 | Ritonavir | MDR1 |
| Dextromethorphan | CYP2D6 | Saquinavir | MDR1 |
| Diazepam | CYP2C19 | Sertinol | CYP2D6 |
| Diclofenac | CYP2C9 | Sertralin | CYP2C19, CYP2C9 |
| Diltiazem | CYP2D6 | Spartein | CYP2D6 |
| Encainid | CYP2D6 | Sulfamethoxazol | CYP2C9 |
| Estradiol | CYP1A2 | Tacrolimus | CYP3A4, CYP3A5, MDR1 |
| Fentanyl | CYP2D6, CYP3A4 | Tamoxifen | CYP2C9, CYP2C19, CYP2D6 |
| Flecainid | CYP2D6 | Taxane | MDR1 |
| Fluconazol | CYP2C9, CYP2C19 | Testosteron | CYP2C9 |
| Fluoxetin | CYP2C9, CYP2C19, CYP2D6 | Thioridazin | CYP2D6 |
| Fluvastatin | CYP2C9, CYP2C19 | Timolol | CYP2D6 |
| Haloperidol | CYP1A1, CYP2D6 | Tolbutamid | CYP2C9 |
| Hydralazin | NAT2 | Torasemid | CYP2C9 |
| Ibuprofen | CYP2C9 | Tramadol | CYP2D6 |
| Imipramin | CYP1A2, CYP2C19, CYP2D6 | Trifluperidol | CYP2D6 |
| Isoniazid | NAT2 | Trimethoprim | CYP2C9, CYP2C19 |
| Lansoprazol | CYP2C19 | Tropisetron | CYP2D6 |
| Lidocain | CYP2D6 | Venlafaxin | CYP2D6 |
| Losartan | CYP2C9 | Verapamil | CYP1A2 |
| Lovostatin | CYP2C9, CYP2C19 | Vincaalkaloide | MDR1 |
| Maprotilin | CYP2D6 | Warfarin | CYP2C9, CYP2C19 |
| Mefenaminsäure | CYP2D6 | Zolmitriptan | CYP1A2 |
| Mexiletin | CYP2D6 | Zuclophentixol | CYP2D6 |
Xenobiotika
Glutathion-S-Transferasen (GST) spielen eine Schlüsselrolle bei der zellulären Detoxifikation von Karzinogenen und Xenobiotika. Genvarianten der GSTs führen zu einer schlechteren Entsorgung der äußerst radikalen Zwischenprodukte aus den Phase I-Reaktionen. Die Untersuchung auf genetische Variationen ist daher angeraten bei verstärkter Schadstoffexposition, insbesondere Kanzerogene. Eine Assoziation von bestimmten Genotypen mit einigen Tumorarten und neurodegenerativen Erkrankungen konnten bereits gezeigt werden.
| GST-T1 | Detoxifiziert u.a. Kanzerogene aus Zigarettenrauch, ist aber auch an der Bildung toxischer Metabolite aus z.B. Dichlormethan beteiligt. Assoziation mit Brustkrebs. Etwa 20 % der kaukasischen Bevölkerung zeigen einen kompletten Funktionsverlust des Enzyms. |
|---|---|
| GST-M1 | Entgiftet u.a. Epoxide. Assoziation mit Brust- und Blasenkrebs. Etwa 50 % der kaukasischen Bevölkerung zeigen einen kompletten Funktionsverlust des Enzyms. |
| GST-P1 | Entgiftet zahlreiche elektrophile Metaboliten. |
Literatur
- Bundesgesundheitsbl – Gesundheitsforsch – Gesundheitsschutz (2004): Genetische Polymorphismen von Fremdstoff-metabolisierenden Enzymen und ihre Bedeutung für die Umweltmedizin. 47:1115-1123
- Schwab, M. et al. (2002): Pharmakogenetik der Zytochrom-P-450-Enzyme. Bedeutung für Wirkungen und Nebenwirkungen von Medikamenten. Deutsches Ärzteblatt 8 (Jg 99).
- Innocenti, F. & Ratain, M.J. (2002): Update on pharmacogenetics in cancer chemotherapy. Eur J Cancer 38: 639-644.