LTT auf SARS-CoV-2-Peptide zum Nachweis der T-lymphozytären Immunantwort auf das neuartige Coronavirus
In der Routine-Labordiagnostik wird hauptsächlich die Antikörperantwort auf das SARS-CoV-2- Virus betrachtet. Antikörper können durch neutralisierende Effekte die Infektion verhindern bzw. die Erregerelimination „unterstützen“. Allerdings entwickeln nicht alle Patienten nach Viruskontakt eine messbare Antikörpermenge, vor allem nicht bei asymptomatischen oder auch milden Verläufen (Mallapaty, 2020; Long et al., 2020;). Zudem verlieren einige Patienten die Antikörperantwort nach Monaten. Die T-zelluläre Antwort spielt hingegen eine zentrale Rolle bei der Virusabwehr, und das T-Zell-Gedächtnis kann über mehrere Jahre persistieren, um gegen schwere Reinfektionen zu schützen (Channappanavar et al., 2014;).
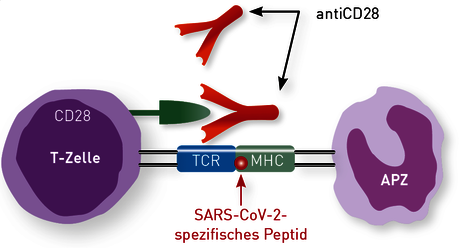
Insofern stellt der Nachweis SARS-CoV-2-spezifischer TZellen eine wichtige Bereicherung der SARS-CoV-2-Labordiagnostik dar. Der LTT auf SARS-CoV-2-Peptide ist im Frühjahr 2020 im IMD Berlin etabliert und gemeinsam mit klinischen Partnern validiert worden. Die Stimulation der Patientenzellen erfolgt mit spezifischen Peptiden, d.h. Gemischen aus kleinen überlappenden Bruchstücken der immuno-dominanten Proteine des Virus (Abb. 1).
Abb. 1 Darstellung der T-Zell-Aktivierung durch Peptide: Das wichtigste Signal für die Aktivierung einer T-Zelle ist die spezifische Erkennung eines Peptids mit dem T-Zell-Rezeptor (TCR). Hierbei muss das Peptid genau „passen“, es gilt also das Schlüssel-Schloss-Prinzip. Für eine vollständige Aktivierung benötigt die T-Zelle zusätzlich noch „Co-Signale“ der Antigen-präsentierenden Zelle (APZ). Dieses Signal wird in vitro bei Peptid-Stimulation unterstützt durch die Gabe von anti-CD28-Antikörpern.
Wann ist ein LTT auf SARS-CoV-Peptide sinnvoll?
Die wichtigste Indikation ist die Frage, ob eine Infektion in der Vergangenheit stattgefunden hat oder ob nach Infektion oder Impfung eine Immunität besteht.
Den LTT sollte man vor allem bei allen Patienten in Erwägung ziehen, die eine fragliche oder fehlende Antikörperantwort nach einer Infektion oder Impfung aufzeigen. Der Antikörpertiter ist zum einen abhängig vom Zeitpunkt der Messung nach Immunisierung, da ein Absinken einige Monate nach Infektion / Impfung häufig beobachtet wird. Zum anderen können Grunderkrankungen oder immunsuppressive Therapien für eine eingeschränkte Antikörperantwort sorgen. Man geht heute davon aus, dass eine T-zelluläre Immunität persistenter ist und mit einem starken Immunschutz einhergeht, sogar bei fehlendem Antikörpernachweis.
Am IMD kann je nach spezifizierter Fragestellung zwischen 2 LTT-Profilen gewählt werden.
Fragestellung 1: Hat mein Patient eine T-Zellimmunität erworben (egal ob durch Impfung oder Infektion)?
Profil: „LTT SARS-CoV-2“ (T-Zell-Reaktion auf Spike-Protein)
Hier werden Peptid-Bibliotheken aus jeweils über 150 Peptiden aus dem C-terminalen Ende (C-Term) und dem N-terminalen Ende (N-Term; enthält RBD-Region) des S-Proteins eingesetzt.
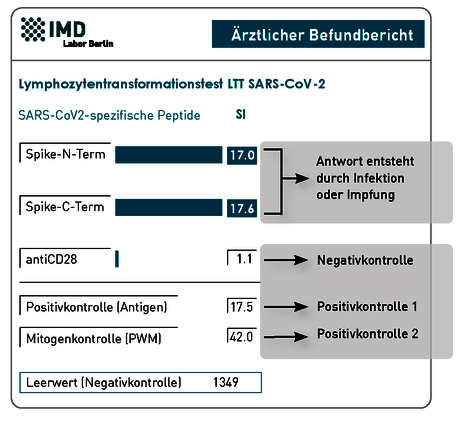
Abb. 2 Beispielbefund für einen positiven LTT auf SARS-CoV-2 Spike-Protein nach vollständiger Impfung
Das N-Term des Spike-Proteins ist sehr spezifisch für SARSCoV-2 (Abb. 2). Eine positive Reaktion im LTT beweist eine Immunantwort auf das SARS-CoV-2-Virus oder das durch die Impfung induzierte Spike-Protein. Im C-Term sind höhere Homologien zu anderen beta-Coronaviren vorhanden, weshalb eine isolierte Reaktivität auf den C-Term eher auf eine Kreuzreaktivität zu endemisch zirkulierenden Erkältungs- Coronaviren (229E, OC43, NL63 und HUK1) hindeutet. Hier gibt es erste wissenschaftliche Erkenntnisse, dass diese Kreuzreaktivität, die in ca 20% der Bevölkerung zu finden ist, eine zumindest teilweise Immunität auch gegen SARSCoV-2 vermitteln könnte (Loyal et. al.).
Mit dem „LTT SARS-CoV-2“ kann somit geprüft werden, ob nach Infektion oder Impfung eine T-Zell-Immunität besteht. Eine Differenzierung zwischen beiden Immunitätsauslösern ist mit diesem Profil jedoch nicht möglich.
Fragestellung 2: Mein Patient ist geimpft, aber hat er dennoch zusätzlich davor oder danach eine SARS-CoV-2-Infektion durchgemacht?
Fragestellung 3: Wie ist die „Bandbreite“ der T-Zellantwort nach durchgemachter Infektion?
Profil: „LTT SARS-CoV-2 Differenzierung“ (T-Zell-Reaktion auf Spike-, Nucleocapsid- und Membranprotein).
Dieses erweiterte Profil zeigt zusätzlich zu dem SpikeProtein im kleineren „LTT-SARS-CoV-2-Profil“ auch die TZellantwort auf das Nucleocapsid- und Membranprotein des Virus auf. Da die bisher in der EU zugelassenen Impfstoffe (Vektor- oder mRNA-Impfstoffe) ausschließlich auf dem Spike-Protein basieren, ermöglicht der „LTT SARS-CoV-2 Differenzierung“ nun als einer der ersten in Deutschland verfügbaren SARS-T-Zelltests eine Unterscheidung, ob die Immunität durch die Impfung oder durch eine vorangegangene oder zusätzliche Infektion entstanden ist (Abb. 3). Da neuere Studien darauf hindeuten, dass die tatsächlich durchgemachte Infektion eine etwas „breitere“ und damit wahrscheinlich stabilere Immunität hinterlässt, könnte diese Aussage z.B. für die Indikationsstellung von Auffrischungsimpfungen hilfreich sein, als eines von mehreren Entscheidungskriterien (Antikörpertiter, Alter, individuelles Risiko durch Grunderkrankungen….).
Abb. 3 Beispielbefund für einen positiven "LTT SARS-CoV-2 Differenzierung" nach erfolgter Infektion.
Spezifität des LTT
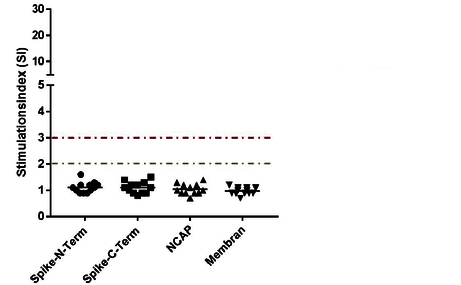
In der Kontrollgruppe (kein Infektionsverdacht, keine Impfung) sind keine Reaktionen auf die einzelnen „Peptid-Bibliotheken“ der Virusbestandteile (Spike-, Nucleocapsid- und Membran-Protein) beobachtet worden. Somit ist die Spezifität als außerordentlich hoch zu bewerten (Abb.4).
Abb. 4 Nicht-Geimpfte und Nicht-Infizierte zeigen keine T-Zellreaktivität im LTT auf SARS-CoV-2-Peptide. Grüne Markierung zeigt den Bereich, ab dem ein grenzwertiges Ergebnis vorliegt (SI zwischen 2 und 3), die rote Markierung zeigt den deutlich positiven Bereich auf (SI >3).
Sensitivität
Nahezu alle in unseren Studien untersuchte nachweislich mit SARS-CoV-2 infizierte Personen (PCR-positiv) oder auch nachweislich vollständig Geimpfte zeigten eine deutliche T-Zellreaktion im LTT auf SARS-CoV-2-Peptide. Auch 1,5 Jahre nach Infektion waren 90 % der Untersuchten im LTT auf SARS-CoV-2 noch deutlich positiv.
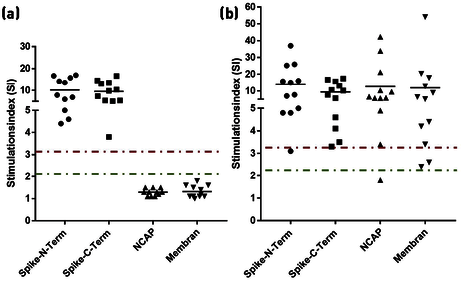
Bei der differenzierten Betrachtung von Geimpften (nachweislich nicht natürlich Infizierten) findet man erwartungsgemäß eine T-Zellantwort auf die N- und C-Term des Spike-Proteins und nicht auf die natürlichen Virusproteine Nucleocapsid (NCAP) und Membran-Protein (Abb. 5a). Eine natürliche Infektion hingegen führt zu einer T-Zellantwort auf NCAP und/oder Membran-Protein. (Abb. 5b).
Abb. 5a / 5b Geimpfte (a) zeigen lediglich eine T-Zellreaktivität auf das Spike-Protein, während Probanden mit durchgemachter Infektion (b) auch auf weitere Virusbestandteile reagieren. Grüne Markierung zeigt den Bereich, ab dem ein grenzwertiges Ergebnis vorliegt (SI zwischen 2 und 3), die rote Markierung zeigt den deutlich positiven Bereich auf (SI >3).
Material
20 ml Heparin- und 5 ml Serum
Der Probenversand erfolgt per Kurier. Bitte kontaktieren Sie unsere kostenfreie Kurier-Hotline unter 030 77001-450.
Abrechnung
Eine Abrechnung ist gegenwärtig nur im privatärztlichen Bereich (GOÄ) gegeben. Die Kosten für Selbstzahler entnehmen Sie bitte dem PDF-Dokument.
Literatur
- Long, Q.X., Tang, X.J., Shi, Q.L., Li, Q., Deng, H.J., Yuan, J., Hu, J.L., Xu, W., Zhang, Y., Lv, F.J., et al. (2020). Clinical and immunological assessment of asymptomatic SARS-CoV-2 infections. Nat Med.
- Mallapaty, S. (2020). Will antibody tests for the coronavirus really change everything? Nature 580, 571-572.
- Channappanavar, R., Fett, C., Zhao, J., Meyerholz, D.K., and Perlman, S. (2014). Virus-specific memory CD8 T cells provide substantial protection from lethal severe acute respiratory syndrome coronavirus infection. J Virol 88, 11034-11044.
- Braun, J., Loyal, L., Frentsch, M., Wendisch, D., Georg, P., Kurth, F., Hippenstiel, S., Dingeldey, M., Kruse, B., Fauchere, F., et al. (2020). SARS-CoV2-reactive T cells in healthy donors and patients with COVID-19. Nature.
- Lucie Loyal , Julian Braun, Larissa Henze, Beate Kruse, Manuela Dingeldey, Ulf Reimer, Florian Kern, Tatjana Schwarz, Maike Mangold et al. (2021). Cross-reactive CD4 + T cells enhance SARS-CoV-2 immune responses upon infection and vaccination. Science