Post Covid- /Post Vac-Syndrom
Bis zu 5% Patienten leiden nach einer akuten SARS CoV-2-Infektion an verschiedenen Langzeiterkrankungen, die als Post-COVID-Syndrom (PCS) bezeichnet werden. Ähnliche Symptome können auch nach Impfungen auftreten und werden dann als Post-Vac-Syndrom bezeichnet, wobei nach heutigem Verständnis die Pathophysiologie beider "Syndrome" ähnlich ist. Die Prävalenzen in der Literatur schwanken, weil die Zahlen abhängig von den Studienkollektiven variieren.
Die Symptome sind sehr vielfältig
Häufige Symptome sind anders nicht erklärbare Müdigkeit und Fatigue, Leistungsdefizite und kognitive Störungen wie z.B. Einschränkungen, insbesondere des Kurzzeitgedächtnisses, Kopfschmerzen, Schlafstörungen sowie Riech- und Schmeckstörungen. Das Spektrum der berichteten Symptome ist aber viel breiter, dazu zählen z.B. pulmonale, kardiovaskuläre, hämatologische, rheumatologische, dermatologische und endokrinologische Symptome, die auch, aber nicht nur, in Abhängigkeit vorbestehender Grunderkrankungen auftreten.
Post-COVID kommt bei Patienten mit symptomatischer als auch mit asymptomatischer SARS-CoV-2-Infektion vor. Bei Post-Vac sind Fälle beschrieben, die an den Tagen nach der Impfung systemische Nebenwirkungen zeigten aber auch solche, die diese problemlos "vertragen" haben. Für das Post-COVID-Syndrom sind als Risikofaktoren neben der Schwere der akuten SARS-CoV-2-Erkrankung, das weibliche Geschlecht und ein erhöhter BMI (Body-Mass-Index) beschrieben. Weiterhin wurden Risikofaktoren identifiziert, die zum Zeitpunkt der COVID-19-Diagnose vorlagen, dazu gehören Typ 2-Diabetes, EBV-Virämie, sehr hohe SARS-CoV-2-Viruslast und positive Autoantikörper-Befunde.
Hyper- und hypoentzündliche Verläufe sind möglich
Viele Studien haben gezeigt, dass bei den Betroffenen proentzündliche Zytokine bis zu mehreren Monaten nach Infektion noch deutlich erhöht nachgewiesen werden können. Hierzu zählen IL-6, TNF-α, IL-1β sowie IFN-γ und auch der Mastzellmarker Histamin. Zudem zeigen sich häufig thromboembolische Veränderungen (Erhöhung der D-Dimere!) und eine Endothelzellaktivierung bzw. latente Endothelitis, was die bei Post Covid nachgewiesenen erhöhten Serumspiegeln von sCD40-Ligand und VEGF erklären kann. Allerdings zeigen nur etwa 80% der Betroffenen diese "hyperinflammatorische Verlaufsform". Etwa 20% der Patienten mit Post Covid und auch Post Vac zeigen keine Entzündungszeichen im Blut und keine Aktivierung von T-Lymphozyten (hypoinflammatorischer Typ).
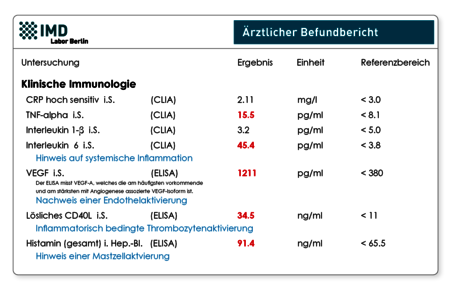
Die Differenzierung in die hyper- und hypoinflammatorische Form ist wichtig
Vor allem wenn sich eine T-zelluläre Immundefizienz manifestiert, kann eine immunmodulierende Therapie angezeigt sein. Dafür ist es wichtig zu wissen, welcher Post-Covid- bzw. Post-Vac-Typ vorliegt. Bei hyperinflammatorischem Geschehen (erhöhte Zytokine im Blut) sollte nicht immunstimulierend therapiert werden, weil sonst durch die Therapie die Symptome noch verstärkt werden. Hier ist eher eher antientzündliche und antioxidative Therapie angezeigt. Dagegen ist bei hypoinflammatorischem Geschehen die Aktivierung von Immunzellen durch Immunstimulanzien mit dem Ziel der Verbesserung der Immunfunktion ein probates Mittel um die Genesung zu beschleunigen.
Störungen im zellulären Immunsystem
In zahlreichen Studien wurde gezeigt, dass bei der Mehrzahl der Betroffenen Störungen im T-zellulären Immunsystem vorhanden sind. Dieses "Postinfektionssyndrom" kannte man, auch wenn es damals Einzelfälle waren, auch vor Corona z.B. von der EBV- oder CMV-Infektion oder nach klassischen Impfungen. Typisch ist eine gestörte Funktionalität der T-Lymphozyten (sichtbar im LTT-Immunfunktion), eine TH2-Dominanz mit erhöhtem IL-4 und vermindertem IFN-g nach Mitogenstimulation (gestörte TH1/TH2-Balance), eine verminderte Funktion der Natürlichen Killerzellen und eine Reduktion der regulatorischen T-Zellen. Letzteres gilt als eine Ursache von Autoimmunität. Eigene Untersuchungen zeigten bei etwa 20% der Betroffenen eine Aktivierung der T-Lymphozyten (HLA-DR+ auf T-Zellen) bei gleichzeitiger funktioneller Erschöpfung und Immunoseneszenz (v.a. der CD8-Zellsubpopulationen), was im quantitativen Immunprofil nachweisbar ist.
Immun-Pathophysiologie des Post-COVID-Syndroms
Zu den derzeitigen Hypothesen, die sehr wahrscheinlich oft in Kombination auftreten, gehören:
- Die Auslösung einer gestörten Immuntoleranz und damit einhergehender Autoimmunität nach der akuten Virusinfektion (Post-Covid) bzw. durch die Auseinandersetzung mit dem Impfantigen (Post- Vac) . Dieser Mechanismus ist nicht spezifisch für SARS-CoV-2. Für viele Viren ist beschrieben, dass sie Trigger von Autoimmunerkrankungen sein können. Gleiches gilt für andere Vaccine.
- mikro-/und makrovaskuläre thromboembolische Ereignisse und nicht reparierte Gewebeschäden
- eine Dysbiose des intestinalen Mikrobioms
- reaktivierte Virusinfektionen, wie z.B. CMV, EBV oder andere Herpesviren
- persistierende SARS-CoV-2-Viren oder freie Spike-Proteine in Geweben oder im Blut. Bisher ist unklar, inwieweit diese an der chronischen Entzündung oder der T-Zellaktivierung beteiligt sind.
Autoimmunität
Die Bildung von Autoantikörpern ist meist Folge einer gestörten Regulationsfunktion der T-Lymphozyten, v.a. der regulatorischen T-Zellen (Treg), in Kombination mit lokalen und systemischen Entzündungsprozessen. Verschiedene Autoantikörper (AAk), insbesondere aber antinukleäre Autonatikörper (ANA), wurden bei akuter COVID-19-Erkrankung nachgewiesen. Es gibt viele Hinweise darauf, dass das Vorhandensein von Autoantikörpern zum Zeitpunkt der COVID-19-Diagnose mit dem Auftreten von Post-COVID-Syndrom assoziiert ist.
Interessant sind Studien an Patienten mit verschiedenen Post-COVID-Symptomen, einschließlich neurologischer und kardiovaskulärer Symptome, die zeigten, dass bei allen Patienten AAk gegen verschiedene G-Protein-gekoppelte Rezeptoren (GPCR) nachweisbar waren. Diese wirken als Rezeptoragonisten, v.a. im vegetativen Nervensystem. Einige dieser regulatorischen GPCR-AAk aktivierten ihre Zielrezeptoren und verursachten einen positiv chronotropen Effekt, wie es die natürlichen Liganden z.B. Angiotensin-2 oder Endothelin-1 tun würden. Andere wiederum verursachten einen negativen chronotropen Effekt. GPCR-AAk wurden mit zahlreichen Symptomen des kardiovaskulären, pulmonalen, intestinalen und zentralen Nervensystems sowie mit Autoimmunerkrankungen in Verbindung gebracht und könnten auch bei der Entstehung von Post-COVID-Symptomen eine kausale Rolle spielen.
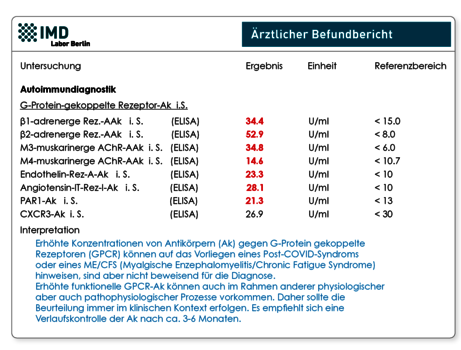
Ebenso wurde untersucht, ob ACE2-AAk dazu beitragen, Post-COVID auszulösen. ACE2, ein membrangebundenes Protein, ist der molekulare Rezeptor für das SARS-CoV-2-Virus. Interessant ist, dass die Konzentration des löslichen ACE2, aber auch der ACE2-AAk mit dem Schweregrad des Post-COVID-Syndroms korrelieren.
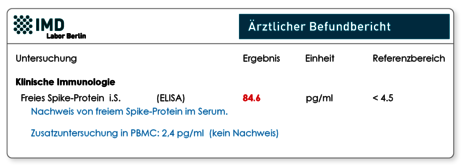
Persistierendes SARS-CoV-2 Spike-Protein
Frei zirkulierendes Spike-Protein steht im Verdacht, für die Entwicklung einer Myokarditis nach SARS-CoV-2 mRNA-Impfung mit ursächlich zu sein. Der Verdacht gründet auf einer Studie, die im Blut von geimpften Myokarditis-Patienten, nicht aber der ebenfalls geimpften Kontrollgruppe, freies Spike-Protein nachweisen konnte (Yonker LM. Circulation. 2023;147:867–876). Inwieweit sich diese Beobachtung auf die Infektion mit SARS-CoV-2 übertragen lässt und ob eine Assoziation mit dem Post-COVID-Syndrom hergestellt werden kann, ist bislang unklar.
Dysbiose des intestinalen Mikrobioms
Die Auswertung der in unserem Mikrobiomlabor untersuchten Stuhlproben bestätigt die wissenschaftliche Literatur, dass Patienten mit Post-Covid sehr häufig auffällige Erregerbefunde haben und zum Teil deutliche labordiagnostische Hinweise auf eine gestörte Darmpermeablität und intestinale Entzündung. Es ist bisher nicht klar, ob eine vorbestehende Dysbiose für ein Post-COVID prädisponiert oder ob die Veränderungen sekundär bzw. parallel zur Krankheitsentwicklung eintreten. In jedem Fall ist es aber so, dass die verminderte Diversität, das Ungleichgewicht zwischen pro- und antientzündlichen Erregern und eine gestörte Darmbarriere zur Persistenz der systemischen Inflammation und der Störung der Immuntoleranz führen.
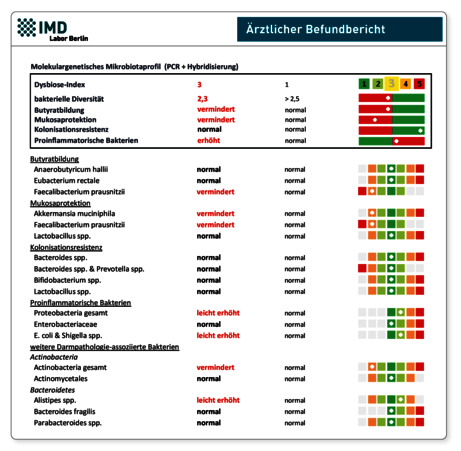
Ansicht vollständiger Stuhlbefund (PDF)
Diagnostikempfehlungen
Es gibt aktuell keine beweisende Labordiagnostik des Post-COVID-Syndroms. Labordiagnostik ist aber differentialdiagnostisch auf Grundlage der klinischen Symptomatik ein wichtiger Baustein, um die Diagnose stellen zu können. Desweiteren dient Labordiagnostik zum Nachweis von Autoimmunität, zur Differenzierung eines hypo- und hyperinflammatorischen Geschehens vor gezielter immunologisch-unterstützender Therapie, zum Nachweis spezifischer (therapierbarer) Veränderungen im Mikrobiom und zur gezielten Substitution von Mikronährstoffen. Letzteres ist wichtig, weil viele Patienten auf Grund des anhaltenden Immunprozesses signifikante Defizite zeigen, die der Genesung wichtigen Autoregulation des Immun-, Entzündungs- und Gerinnungssystems entgegenstehen.
Literatur
- Hilpert K, Mikut R: Is There a Connection Between Gut Microbiome Dysbiosis Occurring in COVID-19 Patients and Post-COVID-19 Symptoms? Front Microbiol. 2021;12:732838
- Ferreira-Junior AS, Borgonovi TF, De Salis LVV, Leite AZ, Dantas AS, De Salis GVV, Cruz GNF, De Oliveira LFV, Gomes E, Penna ALB, De Oliveira GLV. Detection of Intestinal Dysbiosis in Post-COVID-19 Patients One to Eight Months after Acute Disease Resolution. Int J Environ Res Public Health. 2022 19:10189
- Ancona G, Alagna L, Alteri C, Palomba E, Tonizzo A, Pastena A, Muscatello A, Gori A, Bandera A. Gut and airway microbiota dysbiosis and their role in COVID-19 and long-COVID. Front Immunol. 2023; 8;14:1080043.
WEITERE INFORMATIONEN
Die empfohlenen Analysen sind über den Anforderungsbogen COVID 19 / Post-COVID anforderbar.




